Сульфит натрия – это консервант искусственного происхождения, широко применяющийся во многих сферах: он незаменим в пищевой и фармацевтической промышленности, заработал большую популярность в производстве бумаги и тканей. В составе продуктов питания и лекарств его можно распознать под индексом Е221.
Наличия добавки пугаться не стоит – в разумных объемах она не способна принести вред здоровью человека. Для тех, кто старается избегать загадочных Е-шек в своем рационе. Сульфит натрия это пищевая добавка, которая официально разрешена к применению в качестве компонента различных блюд как в Европе, так и в России. Самым важным условием использования консерванта является четкое соблюдение рекомендованных дозировок. Так, безопасным считается сульфит натрия в количестве 0,7 мг на 1 килограмм веса.
Сульфит натрия – это пищевая добавка, которая способна оказывать влияние не только на срок хранения продуктов питания, но также отвечает за их внешнюю привлекательность, регулируя цвет. Кроме того, он способен предотвращать порчу ягод и овощей, выступает в роли хладагента, усилителя цвета и антиоксиданта. При длительном нахождении на открытом воздухе сульфит натрия начинает окисляться. Соединение остается неизменным при контакте с жирами, но легко растворяется в обычной воде, причем чем выше температура жидкости – тем скорее исчезают крупицы.
Содержание
- Что такое сульфит натрия
- Формула сульфита натрия и его свойства
- Получение
- Реакции с сульфитом натрия
- Рекомендованный объем употребления сульфита натрия в составе продуктов питания
- Сферы применения сульфита натрия
- Влияние сульфита натрия на организм человека
- Польза сульфита натрия
- Вред сульфита натрия
- Где можно приобрести сульфит натрия и сколько он стоит
- Заключение
Что такое сульфит натрия
Сульфит натрия – это пищевая добавка, которую производят в лабораторных условиях. Она применяется в разных отраслях промышленности. Так, вещество используют для печати фотографий, производства тканей и вискозного волокна, а также для производства металлоконструкций и бумаги – сульфит натрия помогает достичь требуемого цвета бумаги и картона.
Наиболее часто сульфит натрия применяют в работе с мясом и сухофруктами – он способен значительно продлить срок их хранения и защитить от воздействия вредителей.
Химическая формула сульфита натрия выглядит следующим образом: Na2SO3.
Пищевая добавка считается относительно безопасной для человека и разрешена к применению в странах ЕС и в России. В чистом виде рассматриваемое соединение представляет собой однородный порошок белого цвета, иногда он имеет легкий розоватый оттенок. Запаха вещество практически не имеет, а вот вкус у него выразительный, горько-соленый.
Пищевая добавка представляет собой результат химического взаимодействия диоксида серы с карбонатом натрия. В готовом сульфите натрия могут содержаться дополнительные примеси.
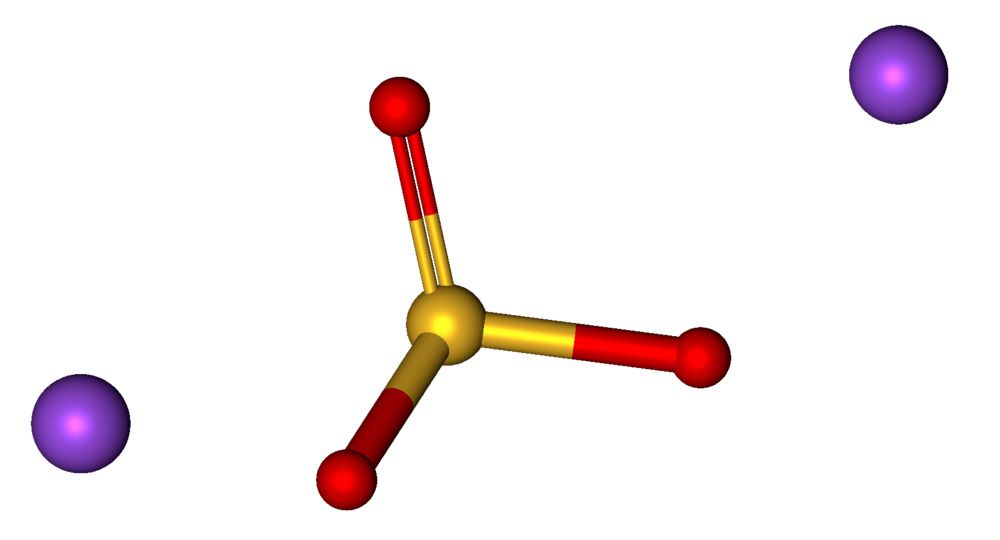
Формула сульфита натрия и его свойства
Формула сульфита натрия выглядит следующим образом:
Na2SO3
Физические свойства
Чистая пищевая добавка визуально представляет собой однородный порошок из белых кристаллов, иногда отдельные частички могут иметь легкий красноватый или розоватый оттенок.
Плотность сульфита натрия – 2,633 г/см3.
Вещество прекрасно растворяется как в холодной, так и в теплой воде. Чем горячее вода, тем быстрее таят крупицы.
Запаха сульфит натрия не имеет, зато обладает ярко выраженным солено-горьким вкусом.
Химические свойства
Сульфит натрия способен прекрасно сохранять свои свойства в нормальных условиях – при температуре в диапазоне от 20 до 25 градусов и невысокой влажности, но при повышении температуры разлагается на две соли. Когда отметка на градуснике достигает показателя в 800 градусов, рассматриваемое вещество разлагается на оксид натрия и диоксид серы.
При высокой степени влажности сульфит натрия окисляется, образуется соль. Для замедления окислительного процесса применяют ингибиторы. В условиях слишком сухого воздуха добавка теряет входящую в ее состав влагу. Е221 полностью обезвоживается при температуре в диапазоне от 150 до 160 градусов.
При воздействии кислорода на сульфит натрия начинается щелочная реакция, в ходе которой выделяется диоксид серы.
Специалисты относят сульфит натрия к категории сильных восстановителей. В водных растворах он присутствует в частично расщепленном состоянии, с легкостью проходит окисление кислородом воздуха, перманганатом калия, бромом и прочими соединениями.
Основные сведения о сульфите натрия:
| Характеристики | Показатели |
| CAS-номер | 7757-83-7 |
| Молекулярная масса, г/моль | 126,0 |
| Плотность, г/см3 | 2,6 |
| Температура, при которой вещество начинает плавиться, °C |
500 |
Получение
В химической промышленности существует несколько методик выделения сульфита натрия.
Так, например, существует метод выделения вещества посредством соединения поваренной соли с сернистым газом и воздействия на них аммиаком. Данный способ целесообразен далеко не во всех сферах промышленности – традиционно его применяют для производства хлористого аммония.
Все реакции проводят исключительно в среде с высоким показателем кислотности.
Выделяют два наиболее распространенных метода получения сульфита натрия: при воздействии повышенных температур и при нормальном температурном режиме. Первый предполагает воздействие на соду увлажненного сернистого газа при температуре в диапазоне от 150 до 170 градусов. Так, данная методика заключается во взаимодействии сухой кальцинированной соды с предварительно увлажненным SO2. В ходе реакции сода сперва преобразуется в сульфит, а затем и в пиросульфит натрия.
Многочисленные эксперименты подтвердили, что сульфит натрия из двух вышеназванных компонентов может быть получен и при более низких температурах в случае правильного подбора объема реагентов.
Как уже было сказано выше, существует и низкотемпературный способ получения сульфита натрия: реакция протекает в диапазоне от 38 до 40 градусов. Гидросульфит натрия соединяют с гидроксидом натрия, в результате чего выделяется сульфит натрия и вода.
Методы получения сульфита натрия:
- Взаимодействие раствора каустической соды (очень едкое вещество) с диоксидом серы (реакция проводится исключительно в лабораторных условиях).
- Взаимодействие сернистого газа с раствором кальцинированной соды.
- Взаимодействие бисульфита натрия с каустической содой при температуре от 38 до 40 градусов.
- Взаимодействие каустической соды с сернистым газом.
Реакции с сульфитом натрия
Большая часть реакций с сульфитом натрия протекает аналогично реакциям других металлов.
Взаимодействие с кислородом с образованием двух молекул натриевой соли:
2Na2SO3 + O2 → 2Na2SO4
Взаимодействие с перекисью водорода с образованием натриевой соли и воды:
Na2SO3 + H2O2 → Na2SO4 + H2O
Взаимодействие с сероводородом с образованием 3 молекул серы, 3 молекул воды и 2 молекул натрия:
Na2SO3 + 2H2S → 3S + 3H2О + 2Na
Взаимодействие с азотной кислотой. В результате образуются оксид азота и вода:
Na2SO3 + 2HNO3 → Na2SO4 + 2NO2 + H2O (t)
Взаимодействие с нитратом серебра с образованием соли серебра и натриевой соли:
2AgNO3 + Na2SO3 → Ag2SO3 + 2NaNO3
Взаимодействие с сульфатом меди с образованием сульфита меди и натриевой соли:
Na2SO3 + CuSO4 → CuSO3 + Na2SO4
Реакция расщепления под воздействием высокой температуры:
4Na2SO3 → 3Na2SO4 + Na2S (t = 600 C)
Рекомендованный объем употребления сульфита натрия в составе продуктов питания
| Категория продуктов питания | Рекомендуемая норма сульфита натрия для человека весом 50 кг в сутки |
| Свежие фрукты | 1,5 г |
| Замороженные фрукты | 25 г |
| Сухофрукты | 50 г |
| Консервированные фрукты | 5 г |
| Джемы | 5 г |
| Фрукты в сахаре | 5 г |
| Фруктовые десерты | 5 г |
| Свежие овощи | 2,5 г |
| Замороженные овощи | 2,5 г |
| Дегидрированные овощи | 25 г |
| Консервированные овощи | 2,5 г |
| Мука | 10 г |
| Крахмал | 2,5 г |
| Свежие морепродукты | 5 г |
| Замороженные морепродукты | 5 г |
| Копченые морепродукты | 1,5 г |
| Белый сахар | 0,75 г |
| Коричневый сахар | 2 г |
| Уксус | 5 г |
| Горчица | 12,5 г |
| Фруктовый сок | 2,5 г |
| Овощной сок | 2,5 г |
| Пиво | 2,5 г |
| Мед | 10 г |
Сферы применения сульфита натрия
Наибольшую популярность рассматриваемое соединение получило в производстве продуктов питания и лекарственных препаратов. Однако вещество применяется и в других отраслях промышленности. Так, например, рассматриваемое соединение применяется для производства целлюлозы, картона и бумаги – оно отвечает за получение требуемой окраски производимой продукции.
Рассматриваемое соединение часто применяют для очистки жидкостей разного назначения: его используют в качестве реагента, забирающего лишний кислород. Дехлорирование жидкости производится посредством добавления в воду специальных таблеток.
Кроме того, добавку используют в качестве гипопрозрачного раствора для очистки фиксированных приборов и предотвращения развития окислительных процессов. Это свойство сульфита натрия обеспечило ему популярность в фотоиндустрии.
Сульфит натрия часто можно встретить в составе косметики: красок для волос, гелей для душа и различных кремов.
В пищевой промышленности рассматриваемая добавка отвечает за поддержание цвета продуктов и увеличивает срок их хранения.
Встретить сульфит натрия можно в составе следующих продуктов питания:
- овощи, фрукты и ягоды в разных формах – свежие, замороженные, консервированные, сушеные, в соусе, сахаре и т.д.;
- различные джемы и варенья, желейные конфеты и конфитюры;
- жидкий пектин;
- консервированные морепродукты;
- специи;
- сладости;
- фруктовые напитки;
- пиво и вино.
Сульфит натрия в роли консерванта
Рассматриваемое соединение обладает массой свойств, которые обеспечили ему популярность в разных отраслях промышленности. Так, например, без добавки не обойтись в работе как со свежими, так и с термически обработанными плодами – благодаря ей продукты хранятся дольше и выглядят лучше.
В качестве консерванта Е221 используют в виноделии, а также в кондитерской промышленности и для производства сухофруктов.
В некоторых государствах, например, в Германии строго запрещено использовать сульфит натрия в работе с мясом и птицей, поскольку соединение способно замаскировать цвет испортившегося продукта.
Влияние сульфита натрия на организм человека
Рассматриваемое соединение, как уже было отмечено выше, широко применяется в обработке продуктов питания. Именно поэтому важно понимать, какое влияние оно оказывает на состояние здоровья и кому стоит воздержаться от регулярного употребления продуктов, содержащих в своем составе Е221.
В разумных объемах добавка абсолютно безопасна: она не вызывает аллергических реакций, привыкания, не сказывается на работе внутренних органов. Но при превышении рекомендуемых дозировок могут возникать следующие реакции: острые боли в животе, тошнота и рвота, нарушения работы ЖКТ, спутанность сознания и даже удушье. Получить вред здоровью при употреблении продуктов питания, в состав которых входит состав натрия, невозможно.
Несмотря на отсутствие вреда, не рекомендуется давать закармливать продуктами с повышенным содержанием сульфита натрия маленьких детей – добавка может вызвать нежелательные изменения здоровья. Так, сульфит натрия способен разрушать витамины, в частности – В1 и Е.
Под воздействием некоторых кислот, в частности – аскорбиновой, сульфит натрия преобразуется в диоксид серы. Это вещество на официальном уровне запрещено к применению в большинстве европейских стран.
Как таковой пищевой ценности сульфит натрия не имеет. Однако рассматриваемая добавка способна нести пользу в качестве одного из компонентов медикаментов. Данное соединение считается особенно эффективным, кода происходит отравление организма тяжелыми солями и металлами – вещество выступает в роли своеобразного антидота, способного минимизировать негативные последствия. Сульфит натрия также способен принести положительный эффект при гипертоническом кризе и хроническом запоре.
Польза сульфита натрия
Научно подтвержденных сведений о пользе сульфита натрия не существует. Однако, как уже отмечалось выше, соединение способно оказывать положительное воздействие на состояние здоровья в составе лекарственных препаратов.
Вред сульфита натрия
Добавка не принадлежит к категории опасных. Если вы употребляете не более 0,7 мг на кг веса в сутки, никакого вреда ваш организм не получит. При попадании в ЖКТ добавка быстро растворяется и выводится через почки.
А вот при превышении рекомендуемого объема сульфита натрия могут возникать аллергические реакции и проявляться негативные симптомы, в числе которых: диарея, нарушение дыхания, тошнота, анафилактический шок.
Где можно приобрести сульфит натрия и сколько он стоит
Проще всего приобрести сульфит натрия в онлайн-магазинах: так у вас будет возможность выбирать не только между желаемым объемом добавки, но также между производителями. Если онлайн шоппинг вам не подходит, обнаружить сульфит натрия вы сможете также в магазине химических реактивов и в отделе фотохимии.
Килограмм сульфита натрия обойдется вам примерно в 300 рублей.
Заключение
Сульфит натрия – это добавка, которую указывают в составе продуктов питания и медикаментов под индексом Е221. Визуально вещество представляет собой мелкие белые кристаллы, иногда они могут иметь слабый розоватый оттенок – окрас зависит от примесей. Запаха сульфит натрия не имеет, а вот вкус у него выраженный, солено-горький.
Наибольшей популярности сульфит натрия достиг в пищевой промышленности: соединение вводят в состав различной фруктовой и овощной продукции – добавка отвечает за поддержание привлекательного окраса плодов и срок ее хранения. Сульфит натрия вводя также в состав мясных и рыбных изделий, муки и сладостей.
Добавку также применяют для производства медикаментов – именно в их составе она способна приносить пользу здоровью человека. В чистом виде сульфит натрия никакой пользы не несет, а вот вред оказать способен – при употреблении слишком большого объема соединения могут возникать аллергические реакции, диарея и прочие отклонения в состоянии здоровья.
Приобрести сульфит натрия проще всего в интернете, однако обнаружить добавку можно и в обычных магазинах. Ее стоимость достигает 300 рублей за килограмм.
Сульфит натрия – это добавка, которая разрешена к применению во всех странах Европейского Союза и России, однако существуют некоторые ограничения. Например, её нельзя добавлять в мясные продукты в Германии, поскольку соединение маскирует цвет испортившегося продукта. Дабы уберечь потребителей от приобретения просроченного мяса и отравления, сульфит натрия запрещен к применению в обработке красного и белого мяса. О других ограничениях неизвестно, но стоит отметить, что специалисты не рекомендуют давать продукты с сульфитом натрия детям.
Читайте также:


























Оставить комментарий